El impacto de la vacunación contra el PRRSV frente a una cepa altamente patógena: el caso de Rosalía
Tiago Nunes1, Salvador Romero1, Lidia de Lucas1, Fernando de Mergelina1, Joel Miranda2
1Global Product Manager, HIPRA
2Global Franchise Manager, HIPRA
Introducción
El virus del Síndrome Reproductivo y Respiratorio Porcino (PRRSV) ha sido una causa importante de brotes de enfermedades desde finales de la década de 1980. Sus efectos en las poblaciones porcinas incluyen fallos reproductivos, problemas respiratorios, tasas de crecimiento más lentas y aumento de las tasas de mortalidad (Zimmerman et al. 2019). Con los años, debido a la alta tasa de mutación y recombinación del virus, han ido surgiendo cepas cada vez más variables, algunas de ellas más agresivas y altamente patógenas, causando brotes aún más graves en diferentes regiones.
En 2020, se identificó en el noroeste de España una nueva cepa altamente patógena de PRRSV, denominada Rosalía. Desde entonces, el impacto productivo y económico de esta cepa ha sido devastador incluyendo una alta mortalidad de cerdas, tasas de aborto persistentemente elevadas (hasta un 27% en un periodo de 17 semanas) y tasas de mortalidad de lechones dramáticamente altas en las transiciones, con picos que oscilaban entre el 28% y el 50% (Martín-Valls et al. 2023).
Aunque se ha demostrado que la vacunación tanto de cerdas como de lechones contra el PRRSV reduce los síntomas clínicos y las pérdidas económicas (Bouchet et al. 2022, Torrents et al. 2020, Linhares et al. 2012), la aparición de la cepa Rosalía ha planteado una pregunta crítica: ¿hasta qué punto son eficaces las vacunas actuales para controlar los brotes causados por esta variante altamente patógena?
Evaluación de la eficacia de la vacunación contra la cepa Rosalía
Un estudio reciente de Cros et al. (2024) exploró la eficacia de una vacuna viva modificada (MLV) en un desafío experimental contra la cepa de PRRS Rosalía. En el estudio participaron 70 lechones naïve PCR y ELISA-negativos a PRRSV, que se dividieron equitativamente en dos grupos. El Grupo A, vacunado intradérmicamente con UNISTRAIN® PRRS a las 3 semanas de edad, se comparó con el Grupo B, que recibió un tratamiento placebo por vía intradérmica (0.2 mL de PBS).
Cinco semanas después de la vacunación, ambos grupos fueron desafiados por vía intranasal con la cepa de PRRS Rosalía (103.55 DICC50/animal). Los signos clínicos, incluyendo letargo, anorexia, estornudos, tos, secreción nasal, disnea y decoloración de la piel se registraron y puntuaron diariamente durante los 28 días después del desafío (sistema de puntuación adaptado de Li et al 2016; Prieto et al, 2011 y Martelli et al, 2009).
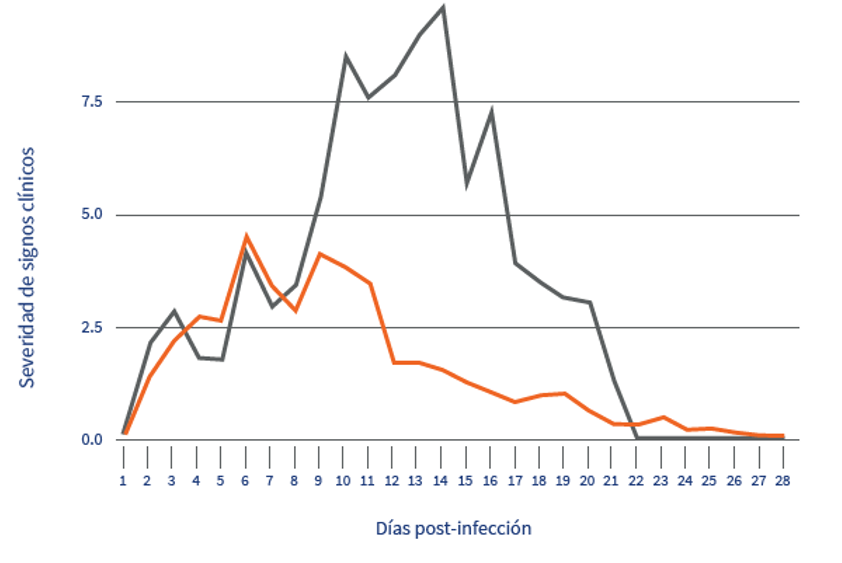
Los resultados revelaron una reducción significativa de los signos clínicos en los animales vacunados (-57%). Estos lechones mostraron síntomas clínicos significativamente más leves, con una puntuación clínica de 1,73, en comparación con 4,04 en el grupo de control (p valor <0,001). Además, la duración de los síntomas clínicos fue notablemente más corta en el grupo vacunado (Figura 1).
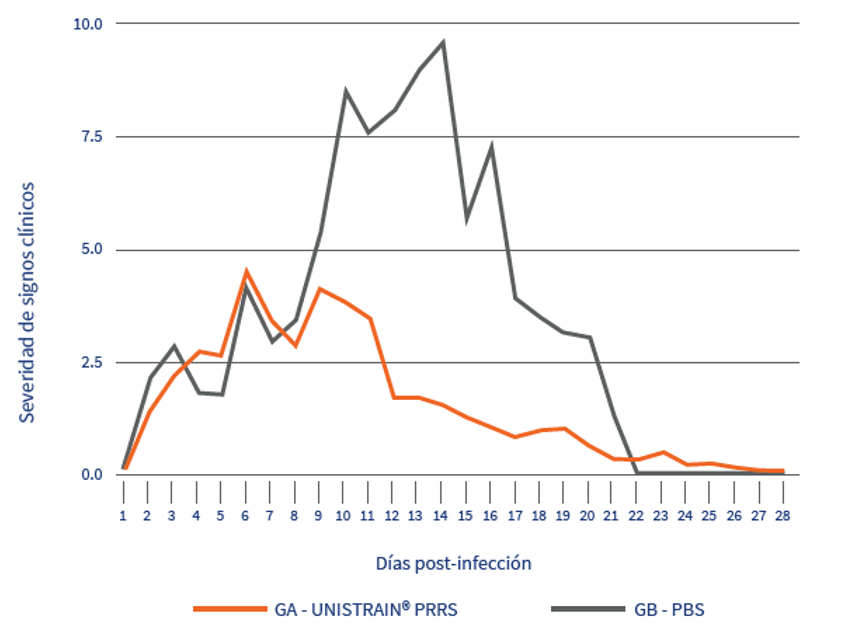
Figura 1 – Signos clínicos después de la infección experimental con HP-PRRSV1 por día y grupo.
La mortalidad también fue registrada y demostró el efecto protector de la vacuna, con una reducción significativa del 89% de la mortalidad en el grupo vacunado (p valor <0,001), que acumuló tan sólo un 8,8% de mortalidad frente a un asombroso 80% en el grupo control. Además, la mortalidad del grupo vacunado se concentró en los 10 primeros días tras el desafío, mientras que la mortalidad del grupo control se prolongó hasta 20 días después (Figura 2).
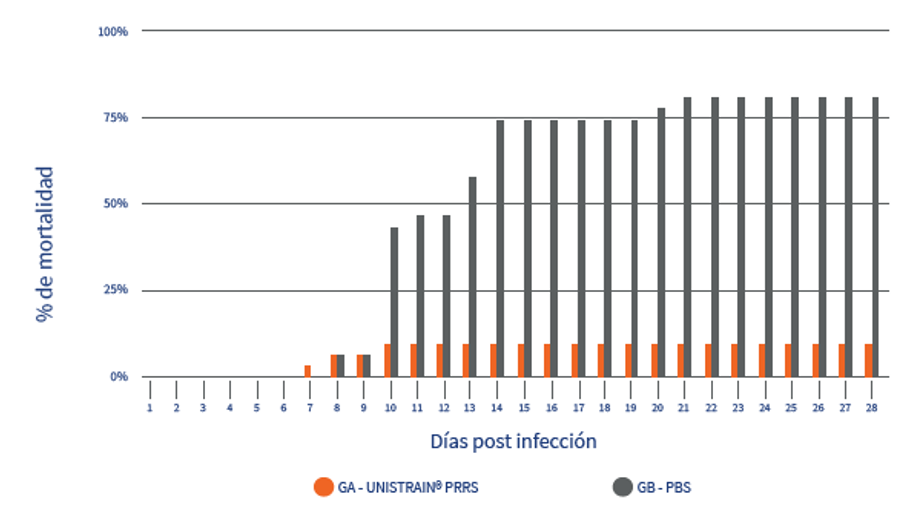
Figura 2 – Mortalidad acumulada después de la infección experimental con HP- PRRSV1 por día y grupo.
Estos resultados muestran un efecto altamente protector de UNISTRAIN® PRRS, siendo hasta donde sabemos, el primer estudio publicado en el que una vacuna previene claramente la mortalidad asociada a la infección por la cepa Rosalía.
Del laboratorio a la granja
En las granjas, varios factores no controlados – como el momento de la infección, la presencia de infecciones secundarias y las condiciones ambientales – pueden influir en la eficacia global de la vacunación. Por lo tanto, para confirmar la efectividad de la vacunación del PRRS contra la cepa Rosalía, es crucial validar estos resultados en condiciones de campo reales.
Un estudio de campo realizado por Meléndez et al. (2024a) evaluó los beneficios de la vacunación en una unidad Wean-to-Finish infectada con cepa altamente patógena Rosalía y localizada en una zona de elevada densidad de granjas de porcino. Se implementó un programa de vacunación intradérmica con el dispositivo HIPRADERMIC® a las 3 semanas de edad utilizando UNISTRAIN® PRRS, y se monitorizaron varios indicadores claves (KPI) antes y después de la vacunación.
Los resultados fueron notables (véase la Tabla 1). El grupo vacunado mostró una reducción significativa de la mortalidad (9,9% frente a 28,3% en el grupo no vacunado, p-valor < 0,001), junto con mejoras en la ganancia media diaria (GMD, +31gr/día) y el índice de conversión (IC, -0,12). Además, se redujeron sustancialmente los costes de medicación en 2,18 €/cerdo. Esto supuso, una reducción del coste de producción de un cerdo desde el destete al sacrificio de 13,49 € cuando se vacunaron.
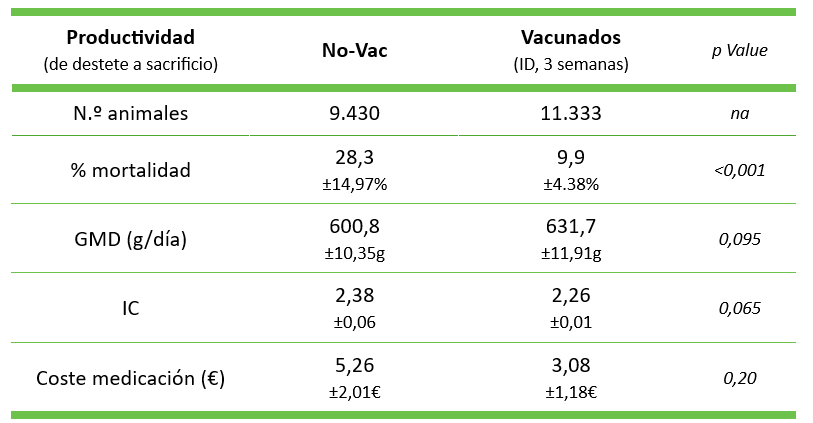
Tabla 1 – Comparación de los KPI’s antes y después de la vacunación con UNISTRAIN® PRRS en una granja Rosalía-positiva. Adaptado de Meléndez et al, 2024(a).
Un estudio similar se realizó en otra granja Wean-to-Finish (Meléndez et al; 2024b), con vacunación intradérmica de lechones a las 3 semanas de edad utilizando UNISTRAIN® PRRS. Además de la reducción de la mortalidad, la mejora significativa en el rendimiento del crecimiento condujo a una reducción de 1,82 €/cerdo en el coste de producción desde el destete hasta el sacrificio (véase tabla 2).
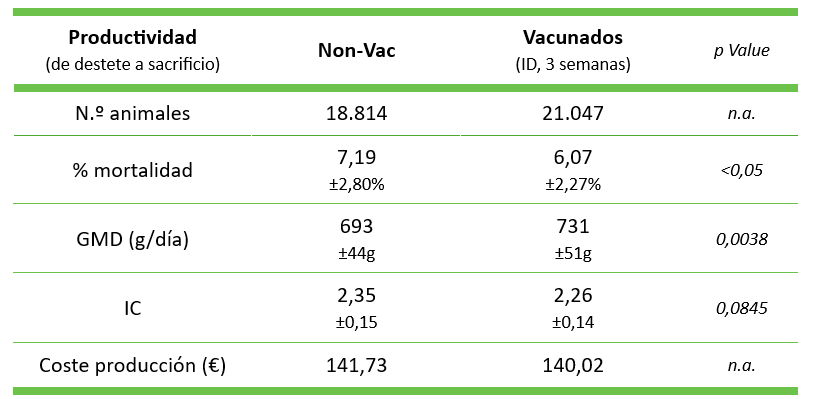
Tabla 2 – Comparación de los KPI’s antes y después de la vacunación con UNISTRAIN® PRRS en una granja Rosalía-positiva. Adaptado de Meléndez et al, 2024(b).
Un tercer estudio de campo publicado por Meléndez et al. (2024c) reforzó estos hallazgos, mostrando una reducción significativa y en menor tiempo, de la carga viral en animales vacunados en una granja positiva a cepa Rosalía, frente a los animales no vacunados: se demostró una reducción del 34% 7 semanas después de vacunar y del 63% a las 12 semanas después de comenzar la vacunación. Una carga viral más baja se asocia con una menor presión de infección, una reducción de los síntomas clínicos y por tanto un mejor rendimiento general, lo que pone aún más de relieve los beneficios de la vacunación, ayudando además a retornar antes a la situación pre-brote.
Conclusiones
A pesar de la naturaleza agresiva y las graves pérdidas económicas asociadas a la cepa Rosalía, la vacunación con UNISTRAIN® PRRS ha demostrado ser eficaz tanto sanitaria como económicamente rentable.
La vacunación de los lechones no sólo reduce significativamente los signos clínicos y la mortalidad, sino que también disminuye la necesidad de tratamientos antimicrobianos y mejora el rendimiento productivo, con un retorno de la inversión positivo para el ganadero. Estos resultados son coherentes con estudios previos en los que la vacunación con UNISTRAIN® PRRS mostró eficacia frente a otras cepas agresivas, como la conocida cepa Lena y cepas altamente patógenas de PRRSV tipo 2 (Bonckaert et al, 2016; Roca et al, 2012).
Los datos disponibles sugieren que los animales vacunados afrontan mejor la infección, mostrando periodos de enfermedad más cortos y una vuelta a la normalidad más rápida. La vacunación sigue siendo una herramienta crítica en la gestión de los brotes de Rosalía, ofreciendo una solución práctica y rentable para mitigar el impacto de esta cepa altamente patógena en la producción porcina.
Si quieres leer más publicaciones sobre PRRS: PRRS Control Publicaciones
Referencias
Bonckaert, C; Van der Meulen, K; Rodríguez-Ballará, I; Pedrazuel Sanz, R; Fenech Martinez, M; Nauwynck, HJ. “Modified-lived PRRSV subtype 1 vaccine UNISTRAIN PRRS provides a partial clinical and virological protection upon challenge with East European subtype 3 PRRSV strain Lena”. Porc Health Manag, 2016:12, 2
Bouchet, F; Berton, P; Teixeira-Costa, C; Lebret, A; Ardies, C; Brissonnier, M; Jeusselin, J; Chevance, C; Normand, V; Boulbria, G. “Economic impact of a porcine reproductive and respiratory syndrome (PRRS) stabilization program in a farrow-to-finish farm using mass vaccination with a modified live vaccine and strict biosecurity measures.” Proceedings – 13th European Symposium of Porcine Health Management. Budapest (HU): ECPHM, 2022. 60.
Cros, S; Pla, H; Simon-Grifé, M; Mergelina, F De; Fenech, M. “Assessment of the efficacy of a live attenuated vaccine against an experimental challenge with a highly virulent PRRSV1 strain.” Allen D. Leman Swine Conference. Saint Paul, MN (USA), 2024.
Li, Z; He, Y; Xu, X; Leng, X; Li, S; Wen, Y; Wang F; Xia, M; Cheng, S; Wu, H. Pathological and immunological characteristics of piglets infected experimentally with a HP-PRRSV TJ strain. BMC Vet Res 12, 230 (2016).
Linhares, DC; Cano, JP; Wetzell, T; Nerem, J; Torremorell, M; Dee, SA. “Effect of modified-live porcine reproductive and respiratory syndrome virus (PRRSv) vaccine on the shedding of wild-type virus from an infected population of growing pigs.” Vaccine, vol 30 (2), 2012: 407-413.
Martelli P, Gozio S, Ferrari L, Rosina S, Angelis E, Quintavalla C, Bottarelli E, Borghetti P. Efficacy of a modified live porcine reproductive and respiratory syndrome virus (PRRSV) vaccine in pigs naturally exposed to a heterologous European (Italian cluster) field strain: Clinical protection and cell-mediated immunity. Vaccine, Volume 27, Issue 28,2009, Pages 3788-3799.
Martín-Valls, GE; Cortey, M; Allepuz, A; Illas, F; Tello, M; Mateu, E. “Introduction of a PRRSV-1 strain of increased virulence in a pig production structure in Spain: virus evolution and impact on production.” Porc Health Manag, 2023: 9, 1.
Meléndez, A; Gayan, J; Sanchez, P; Nodar, L; Lucas, L De; Camarasa, J. “Evolución en el tiempo de la carga vírica de PRRS en un cebadero de animales vacunados y no vacunados infectados con una cepa campo.” XIII Congreso Associación Veterinários de Porcino de Aragón. Zaragoza (ES), 2024b.
Meléndez, A; Mitjavila, D; Escoda, A; Cons, Ll; Nodar, L; De Lucas, L; Camarasa, J. “Beneficios productivos y económicos a nivel de cebo de la vacunación intradérmica de lechones frente a PRRS en una granja española.” XIII Congreso Associación Veterinários de Porcino de Aragón. Zaragoza (ES), 2024c.
Meléndez, A; Nodar, L; Lucas, L De; Torrelles, H; Fernández, V; MArtínez, A; Balliellas, J; Camarasa, J. “Eficacia de la vacunación de lechones en una granja española infectada por cepa de alta virulencia de PRRS.” XIII Congreso Associación Veterinários de Porcino de Aragón. Zaragoza (ES), 2024a.
Prieto C, Martínez-Lobo FJ, Díez-Fuertes F, Aguilar-Calvo P, Simarro I, Castro JM. Immunisation of pigs with a major envelope protein sub-unit vaccine against porcine reproductive and respiratory syndrome virus (PRRSV) results in enhanced clinical disease following experimental challenge. Vet J. 2011 Sep;189(3):323-9. doi: 10.1016/j.tvjl.2010.07.010. Epub 2010 Aug 14. PMID: 20713312; PMCID: PMC7172774.
Roca, M; Gimeno, M; Bruguera, S; Segalés, J; Dìaz, I; Galindo-Cardiel, IJ; Martínez, E; Darwich, L; Fang, Y; Maldonado, J; March, R; Mateu, E. “Effects of challenge with a virulent genotype II strain of porcine reproductive and respiratory syndrome virus on piglets vaccinated with an attenuated genotype I strain vaccine”. The Veterinary Journal, 2012; 193(1):92-6
Torrents, D; Miranda, J; Nodar, L; Martos, A. “Improvement of productive parameters after piglet PRRS vaccination.” Proceedings – 2020 International Pig Veterinary Society Congress. Rio de Janeiro (BR): IPVS, 2020. 535.
Zimmerman, JJ; Dee, SA; Holtkamp, DJ; Murtaugh, MP; Stadejek, T; Stevenson, GW; Torremorell, M; Yang, H; Zhang, J. “Porcine Reproductive and Respiratory Syndrome Viruses (Porcine Arteriviruses).” In Diseases of Swine 11th Ed, by JJ Zimmerman, LA Karriker, A Ramirez, KJ Schwartz, GW Stevenson and J Zhang, 685-708. Hoboken (USA): Wiley Blackwell, 2019.

 Todos los derechos reservados. © HIPRA
Todos los derechos reservados. © HIPRA
