Valutazione della trasmissione iatrogena del virus PSA e PRRS tra suini quando si utilizzano aghi convenzionali e un dispositivo intradermico senza ago
Introduzione
La sindrome riproduttiva e respiratoria dei suini (PRRS), una malattia devastante nei suini caratterizzata da malattia respiratoria e riproduttiva, è presente nel sud-est asiatico (SEA) dagli anni ’90 [1]. Oltre alla PRRS, la diffusione della peste suina africana (PSA) in questa regione della SEA ha aumentato la minaccia per gli allevamenti liberi da PSA [2]. La somministrazione intramuscolare mediante aghi è stata la principale via di vaccinazione nei suini, sebbene i rischi associati agli aghi convenzionali siano elevati. Il virus PRRS (PRRSV), ad esempio, è stato trasmesso da aghi convenzionali ed è stato in grado di indurre la malattia nei suini naïve [3].
Pertanto, gli obiettivi di questo studio erano di valutare la trasmissione del virus della peste suina africana (PSA) e del virus della sindrome riproduttiva e respiratoria suina (PRRSV) tra ago convenzionale e dispositivo senza ago.
Materiali e metodi
Nel presente studio, quarantadue maiali di 3 settimane sono stati acquistati da un allevamento privo di PSA e PRRSV. Gli stati negativi contro entrambi i patogeni sono stati confermati dalla PCR nei campioni di sangue all’arrivo.
Diciotto maiali sono stati assegnati in modo casuale in 6 gruppi di 3 maiali denominati “distributori”, ciascuno denominati IM/ASF, ID/ASF, IM/PRRSV, ID/PRRSV e 2 gruppi di controllo denominati NoChal/IM e NoChal/ID.
Ventiquattro suini di pari età sono stati suddivisi in 4 gruppi “sentinella” di 6 ciascuno e denominati IM/ASFsent, ID/ASFsent, IM/PRRSVsent e ID/PRRSVsent.
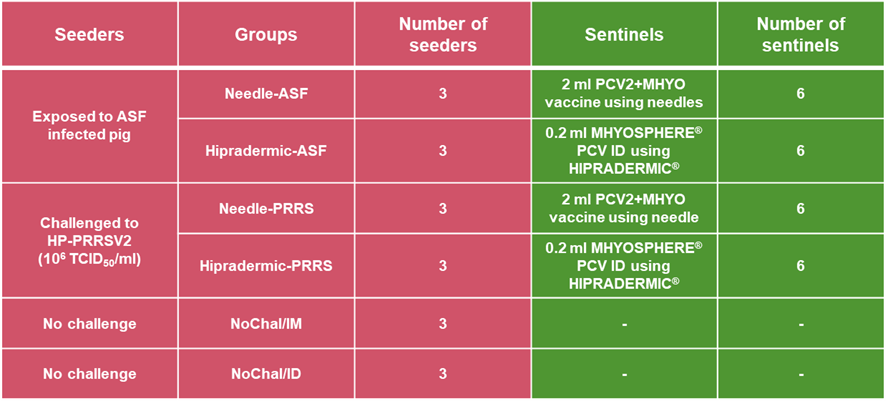
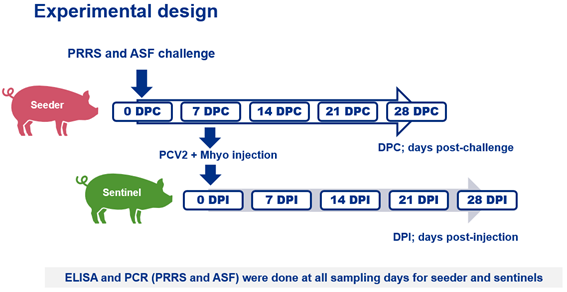
A 0 giorni dall’esposizione (DPE), i gruppi IM/ASF e ID/ASF sono stati esposti a suini infetti da PSA. I gruppi IM/PRRSV e ID/PRRSV sono stati inoculati per via intranasale con 4 ml di HP-PRRSV-2 (106 TCID50/ml, 2 ml/narice).
A 7 DPE (0 giorni dopo l’iniezione (DPI)), i gruppi IM/ASF e IM/PRRSV sono stati somministrati per via intramuscolare con 2 ml di vaccino bivalente di circovirus suino di tipo 2 (PCV2) e Mycoplasma hyopneumoniae (Mhyo) utilizzando aghi convenzionali. I gruppi ID/ASF e ID/PRRSV sono stati somministrati per via intradermica con 0,2 ml di vaccino PCV2 e Mhyo (MHYOSPHERE® PCV ID, HIPRA) utilizzando un dispositivo senza ago (Hipradermic®, HIPRA).
Inoltre, a 7 DPE sono stati utilizzati gli stessi aghi convenzionali e lo stesso dispositivo senza ago per iniettare lo stesso volume di vaccino agli animali dei gruppi sentinelle (1 maiale esposto a 2 sentinelle) con la stessa via di iniezione per ciascuno. I campioni di sangue sono stati raccolti dal gruppo “distributori” a 0, 7, 14, 21 e 28 DPE e dalle sentinelle a 0, 7, 14, 21 e 28 DPI.
Risultati
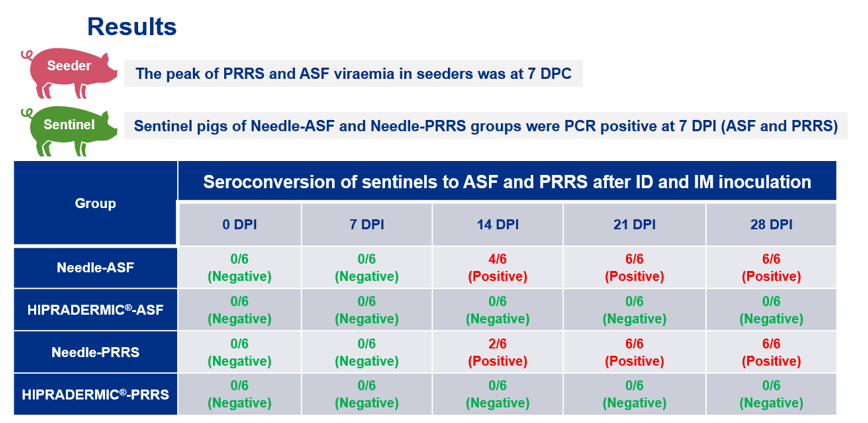
I risultati hanno dimostrato che i gruppi di “distributori” ASF e PRRSV avevano la viremia più alta a 7 DPE. Dopo l’iniezione, i suini “sentinella” dei gruppi IM/ASFsent e IM/PRRSVsent erano positivi alla PCR a 7 DPI. Al contrario, i suini “sentinella” di entrambi i gruppi ID/ASFsent e ID/PRRSVsent erano negativi alla PCR durante l’esperimento.
I risultati della sieroconversione ci mostrano che i gruppi IM/ASFsent e IM/PRRSsent avevano animali positivi a 14 DPI, d’altra parte, i gruppi ID/ASFsent e ID/PRRSsent erano negativi durante l’esperimento
Discussione e conclusione
I nostri risultati hanno rivelato il potenziale di trasmissione di PSA e PRRSV attraverso l’ago durante la vaccinazione.
In caso contrario, la possibilità di applicare vaccini intradermici con un dispositivo senza ago come HIPRADERMIC® inibisce sia la trasmissione di PSA che di PRRSV e potrebbe essere utilizzata per una via di vaccinazione alternativa evitando il trasferimento iatrogeno di agenti patogeni tra animali con aghi condivisi.
Se vuoi leggere altre pubblicazioni sulla PRRS: Pubblicazioni
Puoi fare la tua domanda! Visita il sito Pig333.com ed invia la tua domanda agli esperti.
Riferimenti
- Nilubol D et al. 2013. Genetic diversity of ORF5 gene of porcine reproductive and respiratory syndrome virus (PRRSV) genotypes I and II in Thailand. 158, 943-53.
- Le V et al. 2019. Outbreak of African Swine Fever, Vietnam, 2019. 25, 1433-1435.
- Madapong A et al. 2021 Safety of PRRSV-2 MLV vaccines administrated via the intramuscular or intradermal route and evaluation of PRRSV transmission upon needle-free and needle delivery. 11, 23107.

Swine Viral Evolution and Vaccine Research Unit, Chulalongkorn University, Thailand.



