Evaluación de la transmisión del virus de la PPA y el PRRS entre cerdos cuando se utilizan agujas convencionales y un dispositivo intradérmico sin aguja
Introducción
El Síndrome Reproductivo y Respiratorio Porcino (PRRS), es una enfermedad devastadora en cerdos caracterizada por enfermedad respiratoria y reproductiva, ha estado presente en el sudeste asiático (SEA) desde los años 90 [1]. Además del PRRS, la propagación de la peste porcina africana (PPA) en esta región del SEA ha aumentado la amenaza para los rebaños libres de PPA [2]. La administración intramuscular mediante agujas ha sido la principal vía de vacunación en cerdos, aunque los riesgos asociados con las agujas convencionales son elevados. El virus PRRS (PRRSV), por ejemplo, fue transmitido por agujas convencionales y fue capaz de inducir la enfermedad en cerdos no expuestos [3].
Por lo tanto, los objetivos de este estudio fueron evaluar la transmisión del virus de la peste porcina africana (PPA) y el virus del Síndrome Respiratorio y Reproductivo Porcino (PRRSV) entre la aguja convencional y el dispositivo sin aguja.
Materiales y métodos
En el presente estudio, se usaron cuarenta y dos cerdos de 3 semanas de edad de una piara libre de PPA y PRRSV. Los estados negativos frente a ambos patógenos se confirmaron mediante PCR en muestras de sangre a su llegada.
Se asignaron al azar dieciocho cerdos en 6 grupos llamados seeders de 3 cerdos cada uno, incluidos IM/ASF, ID/ASF, IM/PRRSV, ID/PRRSV y 2 grupos de control NoChal/IM y NoChal/ID.
Veinticuatro cerdos de la misma edad divididos en 4 grupos de 6 cada uno como centinelas, incluidos IM/ASFsent, ID/ASFsent, IM/PRRSVsent e ID/PRRSVsent.
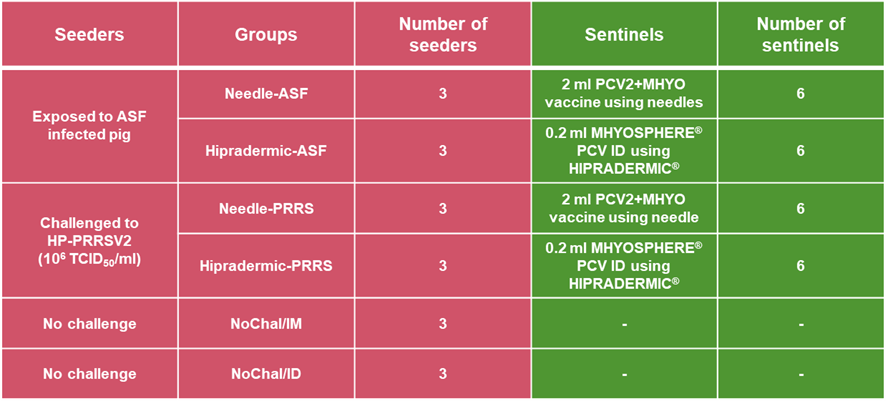
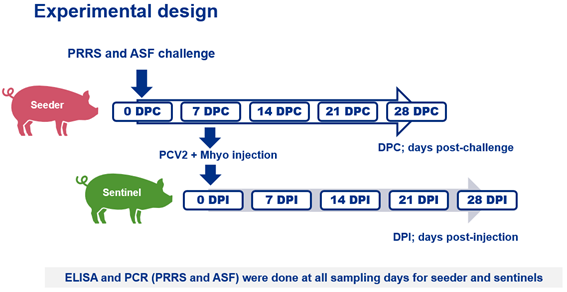
A los 0 días posteriores a la exposición (DPE), los grupos IM/ASF y ID/ASF se expusieron a cerdos infectados con ASF. Los grupos IM/PRRSV e ID/PRRSV se inocularon por vía intranasal con 4 ml de HP-PRRSV-2 (106 TCID50/ml, 2 ml/fosa nasal).
A los 7 DPE (0 días post inyección (DPI)), a los grupos IM/ASF y IM/PRRSV se les administró por vía intramuscular 2 ml de una vacuna bivalente de circovirus porcino tipo 2 (PCV2) y Mycoplasma hyopneumoniae (Mhyo) utilizando agujas convencionales.
A los grupos ID/ASF e ID/PRRSV se les administró por vía intradérmica 0,2 ml de una vacuna PCV2 y Mhyo (MHYOSPHERE® PCV ID, HIPRA) utilizando un dispositivo sin aguja (Hipradermic®, HIPRA).
Además, a los 7 DPE se utilizaron las mismas agujas convencionales y dispositivo sin aguja para inyectar el mismo volumen de la vacuna a los animales de los grupos centinelas (1 cerdo expuesto a 2 centinelas) con la misma vía de inyección para cada uno. Se recolectaron muestras de sangre de seeders a los 0, 7, 14, 21 y 28 DPE, y de centinelas a los 0, 7, 14, 21 y 28 DPI.
Resultados
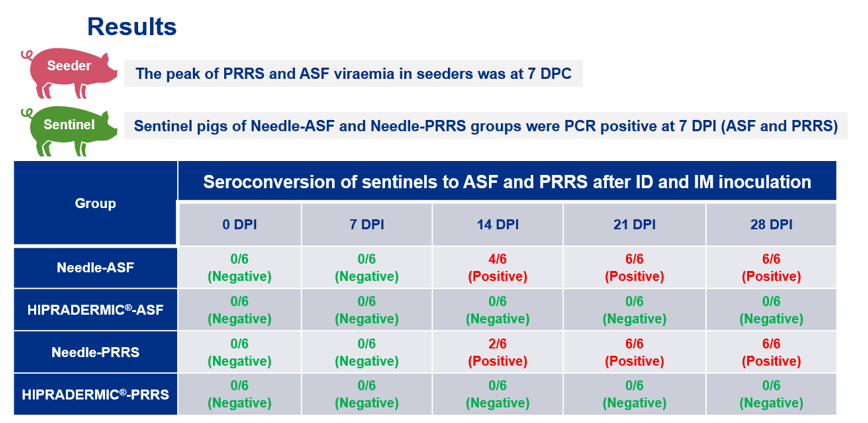
Los resultados demostraron que los grupos de seeders de ASF y PRRSV tenían la viremia más alta a los 7 DPE. Después de la inyección, los cerdos centinela de los grupos IM/ASFsent y IM/PRRSVsent fueron PCR positivos a los 7 DPI. Por el contrario, los cerdos centinela de los grupos ID/ASFsent e ID/PRRSVsent fueron PCR negativos durante todo el experimento.
Los resultados de seroconversión nos muestran que los grupos IM/ASFsent e IM/PRRSsent tuvieron animales positivos a los 14 DPI, por otro lado, los grupos ID/ASFsent e ID/PRRSsent fueron negativos durante todo el experimento.
Discusión y conclusión
Nuestros hallazgos revelaron el potencial de transmisión de PPA y PRRSV a través de agujas durante la vacunación.
De lo contrario, la posibilidad de aplicar vacunas intradérmicas con un dispositivo sin aguja como Hipradermic® inhibe tanto la transmisión de PPA como de PRRSV y podría utilizarse como vía alternativa de vacunación.
Si quieres leer más publicaciones sobre PRRS: Publicaciones
Puedes formular tu propia pregunta! Visita 3tres3.com e introduce allí tu pregunta a los expertos.
Referencias
- Nilubol D et al. 2013. Genetic diversity of ORF5 gene of porcine reproductive and respiratory syndrome virus (PRRSV) genotypes I and II in Thailand. 158, 943-53.
- Le V et al. 2019. Outbreak of African Swine Fever, Vietnam, 2019. 25, 1433-1435.
- Madapong A et al. 2021 Safety of PRRSV-2 MLV vaccines administrated via the intramuscular or intradermal route and evaluation of PRRSV transmission upon needle-free and needle delivery. 11, 23107.

Swine Viral Evolution and Vaccine Research Unit, Chulalongkorn University, Thailand.

 Todos los derechos reservados. © HIPRA
Todos los derechos reservados. © HIPRA
