Se han propuesto varias hipótesis para explicar este fenómeno:
- Modulación en la expresión de moléculas de superficie inmunológicamente relevantes y pobre estimulación de citoquinas:
Tal y como se describió anteriormente, la modulación por parte del virus del PRRS sobre las APC puede interferir en el correcto desarrollo de las respuestas Th1 y Th2. Este hecho provocaría un retraso en la movilización de la inmunidad adaptativa y, consecuentemente, una producción baja de AN. - Existencia de un epítopo de distracción inmunodominante en la GP5 cercano al epítopo neutralizante:
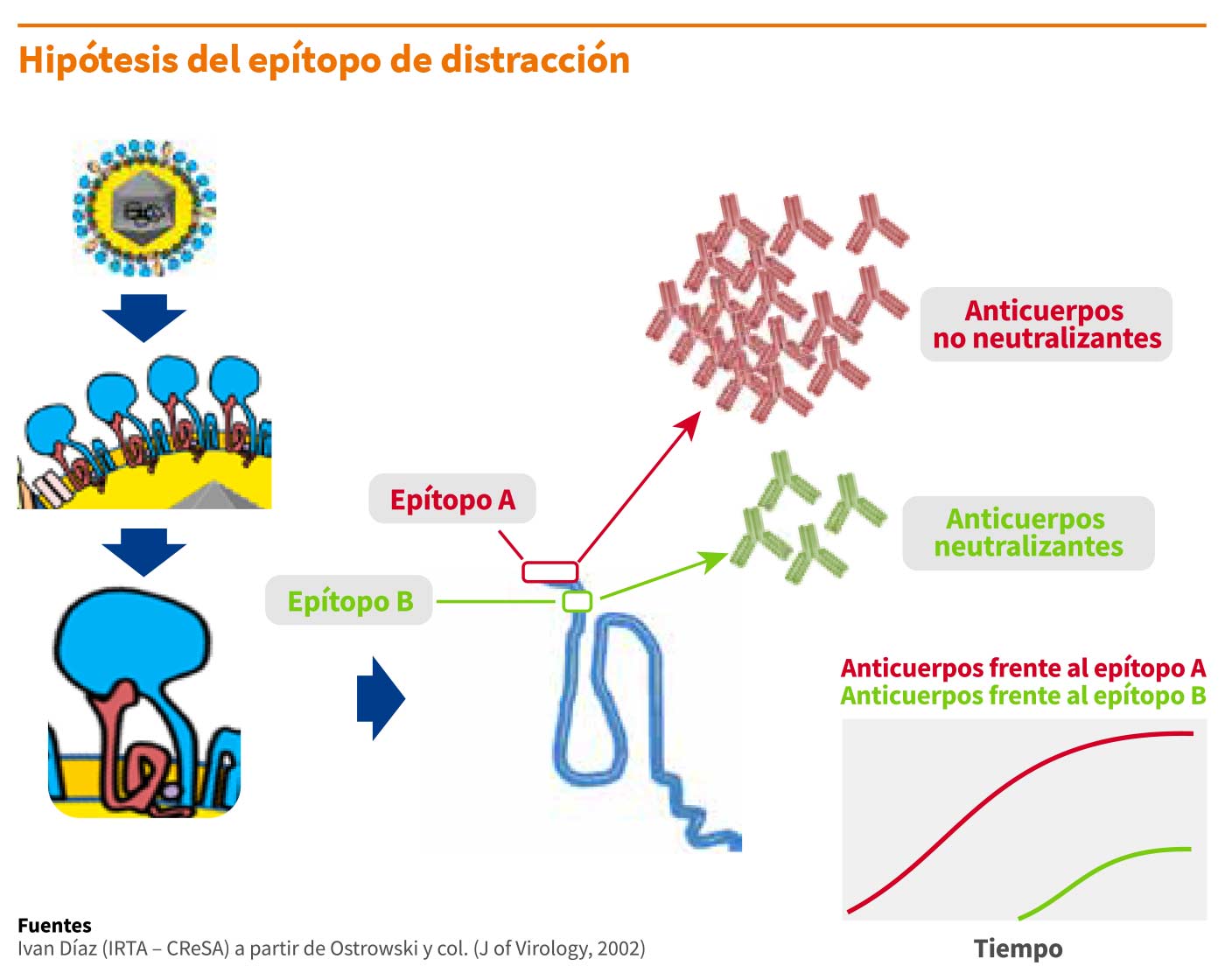
Un epítopo no neutralizante e inmunodominante se localiza cerca de un epítopo neutralizante. La respuesta humoral pronunciada y temprana estaría dirigida en primer lugar hacia el epítopo dominante, mientras que la respuesta frente al epítopo que induce la producción de AN tendría lugar mucho más tarde. - Glicolisación en, o flanqueando, los epítopos neutralizantes:
Las proteínas de membrana están frecuentemente modificadas mediante la inserción de cadenas de azúcar conocidas como glicanos. Los N-glicanos son el tipo de glicanos que se pueden encontrar en el virus del PRRS. La presencia de estos compuestos en los epítopos neutralizantes, o flanqueándolos, puede actuar como un escudo que enmascararía los epítopos e interferiría con la avidez y especificidad de los anticuerpos.
El patrón de localización y la cantidad de estas glicosilaciones varía según los aislados del virus. Se han descrito varios puntos potenciales de glicosilación: hasta 6 en la GP3, hasta 4 en la GP4 y hasta 4 en la GP5 (un máximo de 3 en PRRSV1 y de 4 en PRRSV2).
Curiosamente, los estudios que han usado cepas de campo y los respectivos mutantes desprovistos de glicosilaciones han observado que los títulos de AN son mayores cuando los cerdos se infectaban con los mutantes. Además, en presencia de AN preformados, los mutantes eran mucho más susceptibles a la neutralización. - Proliferación y desarrollo anormal del repertorio de linfocitos B:
El virus del PRRS induce la activación policlonal de linfocitos B y una adenopatía linfoide. Aparentemente, existe una pérdida de la subpoblación de linfocitos B activados (CD2- CD21-) en los cerdos infectados, lo cual se traduce en una pobre maduración de la afinidad y de la generación de células de memoria. - Diversidad genética:
La elevada diversidad genética del virus también podría desarrollar un papel importante. Durante la infección se crean de forma continua mutantes que pueden escapar de la respuesta inmunitaria e impedir el correcto desarrollo de los AN.
En este sentido, se ha observado también que las variaciones en las ORF2-4 y ORF5-6 durante fases tempranas de la infección pueden incrementar la resistencia frente a los AN.


 Todos los derechos reservados. © HIPRA
Todos los derechos reservados. © HIPRA
